造血干细胞(hemopoieticstemcellHSC)是存在于造血组织中的一群原始造血细胞,它不是组织固定细胞,可存在于造血组织及血液中。造血干细胞在人胚胎2周时可出现于卵黄囊,妊娠5个月后,骨髓开始造血,出生后骨髓成为干细胞的主要来源。在造血组织中,所占比例甚少。现代医学中,造血干细胞在骨髓移植和疾病治疗方面有重要作用。
1988年法国的Gluckman教授在国际上率先成功采用脐血造血干细胞移植,救治了一名贫血患儿,标志着脐带血造血干细胞移植时代的开启。全球现每年约进行 6 万例骨髓移植术,其中使用自体和同种异体造血干细胞完成骨髓移植术的患者人数分别为近3.5 万和 2.5 万例。
造血干细胞的来源主要包括骨髓、外周血和脐带血。如今,“骨髓移植”已渐渐被“外周血造血干细胞移植”代替。也就是说,现在捐赠骨髓已不再抽取骨髓,而只是“献血”了。 脐带血是胎儿娩出断脐后残留在脐带和胎盘中的血液,富含造血干细胞,可用于治疗急、慢性白血病和某些恶性肿瘤等多种重大疾病。
基于此,小编针对近年来造血干细胞研究取得的进展进行一番梳理,以飨读者。
1.Nature:重大突破!揭示维生素C调节造血干细胞功能阻止白血病产生机制
doi:10.1038/nature23876

人们对干细胞代谢的了解并不太多,但是来自美国德州大学西南医学中心儿童医学中心研究所的一项新的研究发现造血干细胞摄取非常高水平的维生素C,从而调节它们的功能和抑制白血病产生。相关研究结果于2017年8月21日在线发表在Nature期刊上,论文标题为“Ascorbate regulates haematopoietic stem cell function and leukaemogenesis”。
论文通信作者、德州大学西南医学中心主任Sean Morrison博士说,“一段时间以来,我们已知具有较低维生素C水平的人具有增加的癌症风险,但是我们并没有充分地理解其中的原因。我们的研究提供部分解释,至少从造血系统的角度而言。”
在过去,人们很难研究干细胞代谢,这是因为进行代谢分析需要大量的细胞,然而在体内每个组织中的干细胞是非常少的。在这项新的研究中开发的技术允许科学家们常规地测量干细胞等罕见的细胞群体中的代谢物水平。
2.Nature:利用聚lox条形码技术追踪造血干细胞命运
doi:10.1038/nature23653
在一项新的研究中,德国癌症研究中心的Hans-Reimer Rodewald和他的合作者们想要捕捉血细胞形成中的动态事件,而不仅是拍照。通过与干细胞生物学家Thomas Höfer领导的一个团队密切合作,这些研究人员开发出一种新的技术,从而能够让他们准确地追踪细胞的发育过程。为此,他们给造血干细胞标记上一种基因条形码以便随后能够清晰地鉴定出它们的后代细胞。相关研究结果于2017年8月16日在线发表在Nature期刊上,论文标题为“Polylox barcoding reveals haematopoietic stem cell fates realized in vivo”。
Rodewald团队的Weike Pei和Thorsten Feyerabend培育出在基因组中携带这种基因条形码的小鼠。在选择的不编码基因的位点上,这种基因条形码含有9个来自拟南芥的小DNA片段(也被称作代码元件)。这些片段位于10个被称作IoxP位点的基因切割位点的两侧。通过给予一种药物试剂,与IoxP位点相匹配的分子剪刀Cre能够在这些小鼠的造血干细胞中被激活。随后,这些代码元件被随机地重排或切除。Höfer说,“这种随机的DNA条形码产生器能够产生高达180万个基因条形码,我们能够鉴定出在实验中仅出现一次的代码元件。”
这些分析揭示出两个大的发育分枝在小鼠的造血干细胞中开始产生:在一个分枝中,免疫系统的T细胞和B细胞产生;在另一个分枝中,红细胞和多种其他的白细胞如粒细胞和单核细胞会形成。所有这些细胞类型能够由单个造血干细胞产生。Rodewald强调道,“我们的发现证实从多能性造血干细胞开始的层次发育树经典理论对血细胞生成而言是正确的。”
3.Cell:重大进展!维生素C可促进白血病干细胞死亡,有望用于治疗白血病
doi:10.1016/j.cell.2017.07.032
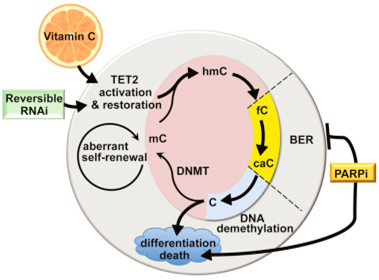
图片来自Cell, doi:10.1016/j.cell.2017.07.032
在一项新的研究中,来自美国纽约大学医学院等研究机构的研究人员发现维生素C不会导致骨髓中存在缺陷的造血干细胞(即白血病干细胞)发生增殖形成血癌,而是促使它们发生分化和凋亡。相关研究结果于2017年8月17日在线发表在Cell期刊上,论文标题为“Restoration of TET2 Function Blocks Aberrant Self-Renewal and Leukemia Progression”。
这些研究人员说,在某些白血病患者中,已知某些基因变化会降低酶TET2促进白血病干细胞分化为成熟的最终会死亡的血细胞的能力。这项新的研究发现维生素C在经过基因改造缺失TET2的小鼠中可激活TET2的功能。论文共同通信作者Benjamin G. Neel说,“我们对高剂量的维生素C可能安全地治疗由TET2缺失性的白血病干细胞导致的血液疾病的前景感到激动人心,而且很可能是与其他的靶向疗法联合使用。”
在10%的急性髓性白血病(AML)患者中存在降低TET2功能的基因突变,在30%的骨髓增生异常综合症中存在TET2基因突变,在将近50%的慢性骨髓单核细胞性白血病中存在TET2基因突变。
4.动物所发现血管微环境调控造血干细胞发育的新机制
doi:10.1016/j.devcel.2017.07.012
在生物体内,微环境同样是造血干细胞多步骤、多阶段发育过程中不可或缺的因素。脊椎动物造血干细胞产生于主动脉-性腺-中肾区,随后迁移到胎肝(小鼠和人)或尾部造血组织(斑马鱼)进行扩增,进而迁移至胸腺向淋系分化,最后迁移至骨髓(小鼠和人)或肾髓(斑马鱼)以维持终生造血。由此可见,在造血干细胞发育的不同阶段,都有特定的微环境对其进行调控。其中,微环境如何调控造血干细胞扩增成为该领域研究的热点问题之一。
鉴于小鼠胚胎子宫内发育和部分突变体早期致死的局限性,中国科学院动物研究所研究员刘峰领导的血液与心血管发育研究组以斑马鱼为模式动物,重点研究和阐释了尾部造血组织中血管内皮细胞对造血干细胞扩增的作用及其机制。研究组充分利用斑马鱼体外发育和早期胚胎透明的优势,通过激光共聚焦显微镜实时观察,发现尾部造血组织处的造血干细胞毗邻于血管内皮细胞,并且其迁移和扩增具有尾部静脉特异的方向性。这一现象暗示尾部血管内皮细胞是造血干细胞微环境中的重要因素。通过对血管内皮细胞、造血干细胞和尾部造血组织中其它细胞类群进行的全基因组表达谱分析,发现一个内皮细胞特异性的转录因子Klf6a。敲低或敲除klf6a会导致斑马鱼尾部造血组织中血管内皮所构成的微环境发生缺陷,从而阻碍了造血干细胞的驻留和扩增。深入的分子机制探索发现,Klf6可以直接调控趋化因子ccl25b的表达,通过Ccl25b/Ccr7 趋化信号影响造血干细胞扩增。另外,小鼠胎肝LSK细胞(Lin-Sca-1+c-Kit+)的体外培养实验结果证明,该分子机制在高等哺乳动物胎肝造血中也是保守的。
5.Nat Cell Biol:揭示脂肪细胞对造血干细胞放化疗后再生的正调控作用
doi:10.1038/ncb3570
2017年7月17日,《Nature Cell Biology》杂志在线发表了中国科学院生物化学与细胞生物学研究所周波研究组和美国德州大学西南医学中心Sean J. Morrison研究组的最新研究成果“Bone marrow adipocytes promote the regeneration of stem cells and haematopoiesis by secreting SCF”(骨髓脂肪细胞通过分泌干细胞因子促进造血干细胞再生)。研究工作揭示了骨髓脂肪细胞对造血干细胞放化疗后再生的正调控作用,颠覆了过去脂肪细胞作为造血抑制物的经典认识。周波研究员为论文第一作者和共同通讯作者,Sean J. Morrison教授为论文另一共同通讯作者。研究同时被评为下期《Nature Cell Biology》杂志封面文章。
成年人腿骨中50%以上的空间被脂肪占据,这一比例在衰老或疾病发生后会进一步增加。骨髓脂肪细胞数量与生理或病理性骨髓抑制具有高度的相关性。因此,一直以来,脂肪细胞抑制骨髓造血被作为教科书般的常识。周波等人的工作发现,骨髓脂肪细胞能够通过分泌造血干细胞必须生长因子SCF促进放化疗后造血干细胞的再生。利用条件性敲除技术将Scf从骨髓脂肪细胞中敲除,会导致放化疗后造血干细胞再生的缺陷,进而降低小鼠的血氧水平和生存率。
6.Leukemia:挑战造血干细胞移植经典法则
doi:10.1038/leu.2017.199
来自北京大学血液病研究所,苏州大学附属第一医院,南方医科大学等处的研究人员发表了题为“Donor and recipient age, gender, and ABO incompatibility regardless of donor source: Validated criteria for donor selection for hematopoietic transplants” 的文章,通过分析上千个病例样品,挑战了HLA全合同胞始终作为首选造血干细胞供者的经典法则。 在这篇文章中,研究人员通过北京大学人民医院等514例HLA全合同胞移植和685例“北京方案”单倍型移植病例,两种类型3年无病生存率分别为74%和75%。多因素分析得到“供受者年龄偏大、女性供男性、供受者ABO血型不合”3个危险因素,累积0-1个、2个、3个危险因素的移植相关死亡率分别为8%,15% 和31%,3年无病生存率为78%,74%和58%,与是否为HLA全合无关。如某中年男性病人如有ABO血型不合、HLA全合的姐姐和血型相合、单倍型相合的儿子,则儿子作为移植供者将很可能优于其姐姐。
这项研究通过1199例连续病例,建立以供受者年龄、性别、血型相合为核心的积分体系,证明该供者选择体系而非经典的人类白血病抗原(HLA)决定移植预后,挑战了HLA全合同胞始终作为首选造血干细胞供者的经典法则。
7.Cell:维生素A缺乏有害于造血干细胞
doi:10.1016/j.cell.2017.04.018
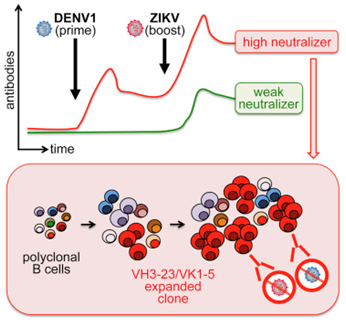
图片来自Cell, doi:10.1016/j.cell.2017.04.018
身体缺乏维生素A对骨髓中的造血干细胞产生有害的影响。如今,在一项新的研究中,来自德国癌症研究中心(DKFZ)和海德堡干细胞研究与实验医学研究所(HI-STEM)的研究人员报道,这种缺乏导致重要的造血干细胞丢失。这一发现为癌症治疗打开新的局面。相关研究结果于2017年5月4日在线发表在Cell期刊上,论文标题为“Vitamin A-Retinoic Acid Signaling Regulates Hematopoietic Stem Cell Dormancy”。
如今,这些研究人员鉴定出视黄酸(维生素A的一种代谢物)是这种过程的一种至关重要的因子。如果这种物质缺乏,那么活性的造血干细胞就不能够返回到休眠状态,相反还会成熟为特化的血细胞。这意味着作为储备的造血干细胞丢失了。这是在利用经过特殊培育的休眠的造血干细胞接受绿色荧光标记的小鼠开展的研究中得到证实的。论文第一作者Nina Cabezas-Wallscheid说,“如果我们给这些小鼠喂食缺乏维生素A的食物一段时间,那么这会导致这些造血干细胞丢失。因此,我们首次能够证实维生素A对造血干细胞产生直接的影响。”
这一发现不仅加强我们对血细胞产生的理解,而且它也有助对之前已证实维生素A缺乏会破坏免疫系统的研究获得新的认识。Cabezas-Wallscheid强调道,“这证实从平衡饮食中摄入数量充足的维生素A是如此至关重要的。人体不能够产生它自己的维生素A。”
8.Nature:重磅!利用血管内皮细胞制造出功能性的造血干细胞
doi:10.1038/nature22326
在一项新的研究中,来自美国威尔康奈尔医学院的研究人员开发出一种创新性方法:利用容易获得的血管内壁细胞无限制地供应健康的血细胞。相关研究结果于2017年5月17日在线发表在Nature期刊上,论文标题为“Conversion of adult endothelium to immunocompetent haematopoietic stem cells”。
论文通信作者、威尔康奈尔医学院安沙瑞干细胞研究所主任Shahin Rafii博士说,“这是一项改变游戏规则的突破,不仅让治疗血液疾病更接近一步,而且也揭示干细胞自我更新机制的复杂生物学性质。”
长期存活的造血干细胞(HSC)能够分化为所有类型的血细胞:白细胞、红细胞和血小板。几十亿个循环流通的血细胞并不会在体内长期地存活,因而必须得到持续补充。当这没有发生时,贫血、流血或危及生命的感染等严重性血液疾病就会发生。HSC的一种特殊的性质是它们也能够“自我更新”形成更多的HSC。这种性质允许仅几千个HSC产生一个人一生当中所需的所有血细胞。 科学家们长期以来希望找到一种方法让身体产生健康的HSC以便治愈这些血液疾病。但是在此之前,还没有人做到这一点,这部分是因为科学家们不能够设计出一种培育环境。仅在这种环境中,干细胞才能够转化为新的可长期存活的细胞。
9.Nature:里程碑突破!首次在实验室利用人多能性干细胞制造出造血干细胞
doi:10.1038/nature22370

造血干细胞分化图,图片来自A. Rad/Wikipedia。
在一项新的研究中,来自美国波士顿儿童医院等研究机构的研究人员首次在实验室中利用能够产生体内几乎任何一种细胞类型的多能性干细胞制造出人造血干细胞。这一进展为研究血液疾病的根本原因和利用病人自己的细胞产生用于治疗目的的免疫匹配性血细胞开辟新的途径。相关研究结果于2017年5月17日在线发表在Nature期刊上,论文标题为“Haematopoietic stem and progenitor cells from human pluripotent stem cells”。
论文通信作者、波士顿儿童医院干细胞移植项目主任George Daley博士说,“我们非常接近于在培养皿中产生真正的人造血干细胞。这项研究是20多年努力的结果。”
尽管利用这些多能性干细胞制造出的细胞是真正的造血干细胞和其他的细胞(即造血祖细胞)的混合物,但是当移植到小鼠体内时,它们能够产生多种类型的人血细胞。
10.Nat Cell Biol:研究揭示造血干细胞的形成过程!
doi:10.1038/ncb3508
像私人侦探一样,St. Jude儿童研究医院的研究人员使用视频监控工具发现了促进血细胞发育的细胞。这项发现为在实验室创造造血干细胞提供了线索,最终可能有助于改善骨髓移植现状。 “这项研究可能为干细胞生物学和血液发育学研究提供了新途径,也为实验室骨髓干细胞移植提供了线索。”St. Jude儿童研究医院血液科助理研究员、论文通讯作者Wilson Clements博士说道。这项研究于近日发表在Nature Cell Biology上。
Clements及文章第一作者Erich Damm发现躯干神经嵴细胞是促使内皮细胞转化为造血干细胞的关键所在。躯干神经嵴细胞由发育中的脊髓生成,会迁移至整个胚胎。它们最终会形成一系列成熟细胞,包括交感神经和副交感神经系统中的神经元、胶质细胞,而交感神经和副交感神经系统控制着人体的喂食、战斗、逃离、生育等过程。
通过使用延时视频,研究人员追踪到了透明的斑马鱼胚胎中神经嵴细胞的迁移。斑马鱼和人类具有几乎一样的血液系统以及使血液系统发育的信号通路。受精20小时后,神经嵴细胞到达了发育中的动脉中,24小时后迁移的细胞与动脉中的内皮细胞接触,然后启动内皮细胞的基因(如runx1)指示它们转化为造血干细胞。
研究人员使用了一系列手段表明扰乱神经嵴细胞的正常迁移或者抑制它们与内皮细胞的接触可以阻止内皮细胞转化为造血干细胞。同时,斑马鱼的其它发育过程不受影响。

